سوال کاربر شیمیپدیا S.I :
سلام. من یه پشت کنکوری نظام قدیم هستم که به یه تناقض علمی رسیدم و واقعا درمونده شدم. خواهش میکنم کمکم کنین.
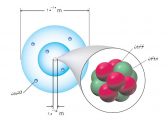
تو شیمی نظام قدیم سال دوم صفحه ۱۸ در تشریح مدل اتمی نیلزبور تو بند های۲و۳و۴و۵ میخونیم:
«۲- انرژی الکترون با فاصله آن از هسته رابطه “”مستقیم”” دارد.
۳- الکترون فقط می تواند در فاصله های معین و ثابتی پیرامون هسته گردش کند. در واقع الکترون فقط اجازه دارد که مقادیر معینی انرژی داشته باشد. به هر یک از این مقادیر انرژی تراز انرژی می گویند.
۴- این الکترون معمولا در “”پایین ترین تراز انرژی ممکن (نزدیک ترین مدار به هسته)”” قرار دارد. به این تراز انرژی حالت پایه می گویند.
۵- با دادن مقدارمعینی انرژی به این الکترون می توان آن را قادر ساخت که از حالت پایه “”(ترازی با انرژی کمتر) به حالت برانگیخته(ترازی با انرژی بالاتر)”” انتقال پیدا کند.»
همچنین در کتاب فیزیک پیش دانشگاهی رشته ریاضی نظام قدیم صفحه ۲۰۸ (در کتاب رشته تجربی صفحه مورد نظر فرق میکند) در تشریح مدل اتمی بور از مدار های مانا صحبت شده بود و در صفحه بعد آن در رابطه ۷-۱۷ می بینیم که انرژی الکترون روی یک مدار مانا با شعاع آن مدار نسبت عکس دارد. حالا من چند سوال دارم:
الف- تراز انرژی و مدار مانا در “”نظریه بور”” چه تفاوتی دارند؟ اگر یکی هستند پس چرا این تناقض در دو کتاب درسی وجود دارد؟ اگر متفاوتند لطفا کمی موضوع را تشریح کنید. آیا در مدل اتمی بور تراز انرژی و مدار الکترون بر هم منطبق هستند؟ چرا انرژی آن ها به عکس هم تغییر می کند؟
ب- انرژی الکترون ناشی از چیست؟ وقتی از انرژی الکترون صحبت میشود، منظور کدام انرژی است؟ چون اگر منظور انرژی ناشی از نیروی الکتریکی متقابل بین هسته و الکترون است، طبیعی است که با افزایش فاصله الکترون از هسته اتم انرژی کاهش یابد. یا مثلا وقتی در صفحه ۶۸ شیمی سال دوم در نمودار شکل ۴ از انرژی بین دو اتم حرف میزنیم منظور کدام انرژی است؟ جنس یا منشا این انرژی چیست؟
پ- آیا رابطه نیلزبور در مورد انرژی الکترون در کتاب فیزیک، برای تراز انرژی در مدل اتمی کوانتومی نیز برقرار است؟ یعنی با افزایش فاصله الکترون از هسته، انرژی آن کاهش می یابد؟ پس چرا در شیمی یاد گرفته ایم لزوما این طور نیست؟ موضوعی که باعث شده اوربیتال های برخی زیرلایه های اتم که فاصله بیشتری از هسته نسبت به زیر لایه قبل خود دارند، زودتر پر شوند.
ت- در صفحه ۲۱ شیمی سال دوم نمودار ‘فکر کنید’ نیز می بینیم با کاهش فاصله الکترون از هسته، انرژی یونش آن افزایش می یابد. لطفا رابطه آن با انرژی ترازهای الکترون و تناقض یاد شده را توضیح دهید.
پاسخ مشاور تحصیلی:
سلام. این تناقض ظاهری که از آن صحبت میکنید در جاهای دیگر نیز بین شیمیدانان و فیزیکدانان دیده میشود. برای مثال کار فشار حجم در شرایط فشار ثابت در شیمی و در فیزیک قرینهی هم هستند! دلیل این موضوع آنست که در شیمی ما معیار را سیستم قرار میدهیم (ناظر سیستم است) و در فیزیک معیار و ناظر آزمایشگر است. بنابراین هرچقدر از هسته دور میشویم، از دید هسته (نگاه شیمیایی) الکترون انرژی بیشتری میگیرد (مثل توپی که مدام ارتفاع آن زیاد میشود و از دید زمین انرژی آن بیشتر میشود). ولی در فیزیک و از دید آزمایشگر انرژی پتانسیل ذخیره شده در سیستم با افزایش فاصله بین الکترون و اتم به طور مرتب کاهش مییابد.
یعنی هم نگاه فیزیکی و هم نگاه شیمیایی درست است ولی از دو منظر متفاوت.
برای اطلاعات بیشتر تماس بگیرید.
مشاوره جهت کلاس شیمی
با برنده مدال طلای المپیاد شیمی و استاد کنکور
- شما میتوانید جهت مشاورۀ شرکت در کلاسهای شیمی کنکور، تقویتی و المپیاد شیمی با برندۀ مدال طلای المپیاد شیمی به صورت مستقیم در تماس باشید!
- فقط در تلگرام: HosseinZamaninasab@
مشاوره رایگان است!